- 产地
- 苏州
- 品牌
- 外泌体提取试剂
- 型号
- 齐全
- 是否定制
- 是
外泌体是指包含了复杂RNA和蛋白质的小膜泡(30-150nm),现今,其特指直径在40-100nm的盘状囊泡。1983年,外泌体初次于绵羊网织红细胞中被发现,1987年Johnstone将其命名为“exosome”。多种细胞在正常及病理状态下均可分泌外泌体。其主要来源于细胞内溶酶体微粒内陷形成的多囊泡体,经多囊泡体外膜与细胞膜融合后释放到胞外基质中。所有培养的细胞类型均可分泌外泌体,且外泌体天然存在于体液中,包括血液、唾液、尿液、脑脊液和乳汁中。有关他们分泌和摄取及其组成、“运载物”和相应功能的精确分子机制刚刚开始研究。外泌体目前被视为特异性分泌的膜泡,参与细胞间通讯,对外泌体的研究兴趣日益增长,无论是研究其功能还是了解如何将其用于微创诊断的开发。这些试剂盒不需要特殊设备,随着产品不断更新换代,提取效率和纯化效果逐渐提高。济南正规外泌体提取试剂

外泌体相关miRNA与肺病的诊断:进一步研究发现,另外6种外泌体(miR-151a-5p、-30a-3p、-200b-5p、-629、-100、-154-3p)可用于肺病的诊断,其AUC为0.76。这些miRNAs具有NSCLC早期诊断的高度敏感性,有望成为NSCLC早期诊断筛查的生物标志物。在临床应用方面,目前ExosomeDiagnostics公司研发的基于血浆外泌体的ALK试剂盒已于2016年初被美国FDA批准用于临床。这是世界上个以血液样本分析外泌体RNA的临床液体活检。这项方法可以准确、实时地检测NSCLC患者的EML4-ALK突变,通过比较NSCLC患者组织ALK水平和相应的血浆样本发现该项检测可以达到88%的诊断灵敏度和100%的诊断特异性。而此前,对于EML4-ALK的检测是基于组织活检的FISH或IHC,而且,FISH缺乏灵敏性,误诊率也较高。成都外泌体提取试剂厂家现货目前人们多采用超速离心、免疫磁珠、超滤、沉淀或试剂盒等方法实现外泌体的提取分离。

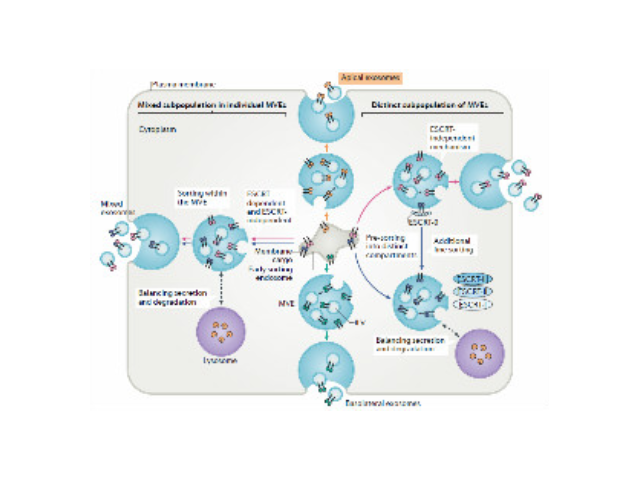
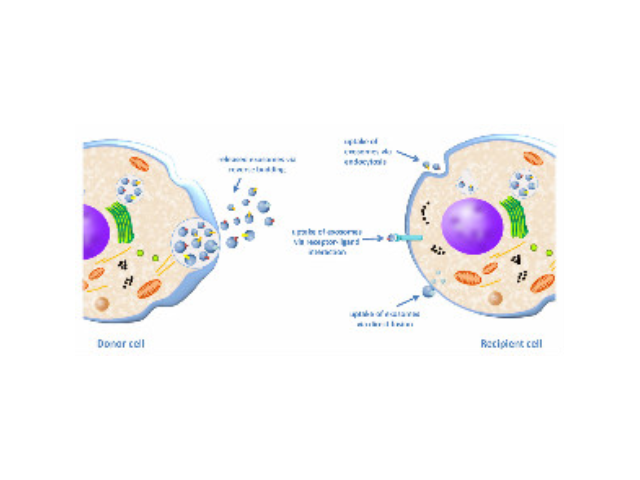
目前的主流观点认为,外泌体的产生过程为:细胞膜内陷,形成内体(endosome),再形成多泡体(multivesicularbodies,MVB),较后分泌到胞外成为外泌体。外泌体中携带有母细胞的多种蛋白质、脂类、DNA和RNA等重要信息。外泌体较早见于1981年,EGTrams等在体外培养的绵羊红细胞上清液中发现了有膜结构的小囊泡,并命名为exosome。对于外泌体的作用,当时推测为细胞排泄废物的一种方式。1996年GRaposo等发现类似于B淋巴细胞的免疫细胞也会分泌抗原呈递外泌体(antigenpresentingvesicle),所分泌的外泌体可以直接刺激效应CD4+细胞的抗一些病症反应。2007年HValadi等进一步发现细胞之间可以通过外泌体中RNA交换遗传物质。随着有关外泌体研究越来越多,研究者发现它普遍参与了机体免疫应答、抗原呈递、细胞分化、一些病症生长于侵袭等各种生物过程中。
外泌体与免疫系统:不同的细胞来源的外泌体,包括免疫细胞(B细胞和树突状细胞)、病细胞、上皮细胞和间充质细胞,释放出带有载体的外泌体,可影响先天免疫系统和适应性免疫系统中受体细胞的增殖和各自的活性。CD4+和CD8+T细胞可直接或间接地受到外泌体的影响,刺激或压制其增殖和功能。外泌体与代谢性和心血管疾病:外泌体可以通过携带miRNA或代谢物分子在代谢性疾病和心血管疾病的发生的发展过程中起作用。体外培养心血管疾病的细胞收集的外泌体与疾病相关的代谢适应有关;体外培养的间充质干细胞和胚胎干细胞的外泌体具有保护心血管的作用。这些发现表明不同来源的外泌体可以通过传递miRNA,蛋白等物质改变受体细胞的代谢状态。如纯度和回收率低,杂蛋白较多(假阳性),颗粒大小不均一,产生难以去除的聚合物。

外泌体:该研究主要是做了牡蛎基因组测序,并揭示其应激适应和壳结构的复杂性。其中涉及,所鉴定的259种壳蛋白中的84%不是经典分泌蛋白;它们可能是细胞的一部分或被外泌体沉积而来。259个壳蛋白中的61个与外泌体数据库中的蛋白质匹配,支持了外泌体的存在。在矿化前缘处观察到含有方解石晶体的细胞和外泌体样囊泡,尽管它们在壳形成中的重要性是有争议的。这项研究为它们在壳内的存在及其可能参与壳形成提供了分子证据。Hedgehog(Hh)蛋白的保守家族作为短距离和长距离分泌的形态发生素,在胚胎发育过程中控制组织构型和分化。成熟的Hh携带疏水性棕榈酸和对其细胞外扩散至关重要的胆固醇修饰。通过密度梯度离心,样品中的外泌体将在1.13-1.19g/ml的密度范围富集。杭州外泌体提取试剂直销价
将人尿液来源细胞的培养基通过0.22微米滤膜过滤,以去除大的细胞残片以及其它杂质。济南正规外泌体提取试剂
多泡内体的腔内囊泡,要么分选进溶酶体将物质降解,要么作为外泌体分泌到胞外环境中。将膜分选到不同的腔内囊泡群中的机制尚不清楚。该研究发现物质被分选到内体膜上的不同子域中,并且外泌体相关结构域向内体腔的转移不取决于ESCRT(运输所需的内体分选复合体)的功能,但是需要鞘脂神经酰胺。纯化的外体富含神经酰胺,并且在神经鞘磷脂酶被压制后外泌体释放减少。这些结果确定了内体内膜运输和外泌体形成的途径。环-GMP-AMP合酶(cGAS)在细菌传染期间检测胞质DNA并诱导抗细菌状态。cGAS信号通过合成第二信使——环GMP-AMP(cGAMP),启动干扰素基因的刺激物(STING)。该研究表明,当它们在cGAS表达细胞中产生时,cGAMP被整合到细菌颗粒中,包括慢细菌和疱疹细菌颗粒。细菌体将cGAMP转移至新传染的细胞并引发STING依赖性抗细菌程序。这些效应**于外泌体和细菌核酸。研究结果揭示了天然免疫信号在细胞间转移的途径,可能加速和扩大抗细菌反应。此外,用装载cGAMP的慢细菌传染树突细胞增强了它们的活化。因此,用cGAMP加载细菌载体对于疫苗开发具有很大希望。济南正规外泌体提取试剂
外泌体的生物学功能研究中需要分离完整的外泌体颗粒,而传统超速离心方法步骤繁琐、硬件要求高、操作难度大。李记生物自主开发的外泌体快速提取试剂盒,组分经过优化处理,适用于细胞培养上清液、血清、血浆、尿液及其他体液(脑脊液、腹水、羊水、乳汁以及唾液等)中的外泌体提取,并搭配纯化过滤装置,可快速高效地获得高纯度外泌体颗粒。注意事项:1.对于待测样品粘度过大时,可将样本用4℃预冷的1×PBS缓冲液进行等体积稀释处理。2.当血清、血浆、唾液等样品收获的外泌体浓度较高,收获的外泌体颗粒无法通过EPF柱纯化时,可用4℃预冷的1×PBS进行稀释后再通过EPF柱离心。超离法因操作简单,获得的囊泡数量较多而广受?欢...
- 石家庄正规外泌体提取试剂厂家 2026-05-03
- 杭州外泌体提取试剂价格 2026-05-03
- 深圳外泌体提取试剂厂家现货 2026-05-03
- 唐山外泌体提取试剂哪家好 2026-05-03
- 珠海正规外泌体提取试剂服务电话 2026-05-02
- 芜湖外泌体提取试剂厂家推荐 2026-05-02
- 郑州外泌体提取试剂厂家 2026-05-02
- 昆明外泌体提取试剂销售厂家 2026-05-01
- 开封外泌体提取试剂哪里买 2026-05-01
- 深圳正规外泌体提取试剂单价 2026-05-01
- 广州外泌体提取试剂平均价格 2026-04-29
- 太原外泌体提取试剂厂家供应 2026-04-29
- 外泌体提取试剂销售厂家 2026-04-29
- 合肥正规外泌体提取试剂平均价格 2026-04-29
- 重庆外泌体提取试剂推荐厂家 2026-04-29
- 太原正规外泌体提取试剂哪里买 2026-04-28


- 原代细胞分离试剂盒销售厂家 05-03
- 成都细胞高效转染试剂销售厂家 05-03
- 重庆细胞外基质胶平均价格 05-03
- 青岛原代细胞分离试剂盒厂家直销 05-03
- 成都正规鼠尾胶原服务电话 05-03
- 深圳外泌体提取试剂厂家现货 05-03
- 昆明原代细胞分离试剂盒厂家直销 05-03
- 上海原代细胞分离试剂盒服务电话 05-03
- 芜湖开封鼠尾胶原 05-03
- 唐山外泌体提取试剂哪家好 05-03