- 品牌
- 司鼎;OriCell
聚合酶链式反应的常见问题:出现非特异性扩增带:PCR扩增后出现的条带与预计的大小不一致,或大或小,或者同时出现特异性扩增带 与非特异性扩增带。非特异性条带的出现,其原因:一是引物与靶序列不完全互补、或引物聚合形成二聚体。二是Mg2+离子浓度过高、退火温度过低,及PCR循环次数过多有关。其次是酶的质和量,往往一些来源的酶易出现非特异条带而另一来源的酶则不出现,酶量过多有时也会出现非特异性扩增。其对策有:必要时重新设计引 物。减低酶量或调换另一来源的酶。降低引物量,适当增加模板量,减少循环次数。适当提高退火温度或采用二温度点法(93℃变性,65℃左右退火与延伸)。聚合酶链反应应经常使用带有一次性柱塞和超长移液器吸头的移液器。苏州特殊样本荧光PCR
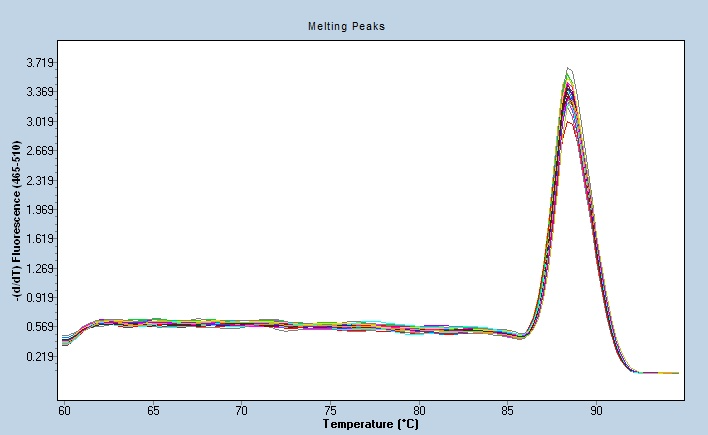
聚合酶链式反应的常见问题:靶序列或扩增产物的交叉污染:这种污染有两种原因:一是整个基因组或大片段的交叉污染,导致假阳性。这种假阳性可用以下方法解决:操作时应小心轻柔,防止将靶序列吸入加样内或溅出离心管外。除酶及不能耐高温的物质外,所有试剂或器材均应高压消毒。所用离心管及样进头等均应一次性使用。必要时,在加标本前,反应管和试剂用紫外线照射,以破坏存在的核酸。二是空气中的小片段核酸污染,这些小片段比靶序列短,但有一定的同源性。可互相拼接,与引物互补后,可扩增出PCR产物,而导致假阳性的产生,可用巢式PCR方法来减轻或消除。苏州特殊样本荧光PCR热启动聚合酶链式反应可以通过将反应组分加热到变性温度在加入聚合酶之前。

聚合酶链式反应(PCR)是一种用于放大扩增特定的DN段的分子生物学技术,它可看作是生物体外的特殊DNA复制,PCR的很大特点是能将微量的DNA大幅增加。因此,无论是化石中的古生物、历史人物的残骸,还是几十年前凶杀案中凶手所遗留的毛发、皮肤或血液,只要能分离出一丁点的DNA,就能用PCR加以放大,进行比对。这也是“微量证据”的威力之所在。由1983年美国首先提出设想,1985年由其发明了聚合酶链反应,即简易DNA扩增法,意味着PCR技术的真正诞生。到2013年,PCR已发展到第三代技术。
聚合酶链式反应:反应的控制:PCR反应的缓冲液 提供合适的酸碱度与某些离子;镁离子浓度 总量应比dNTPs的浓度高,常用1.5mmol/L;底物浓度 dNTP以等摩尔浓度配制,20~200umol/L;TaqDNA聚合酶 2.5U(100ul);引物浓度一般为0.1 ~ 0.5umol/L;反应温度和循环次数;变性温度和时间 95℃,30s;退火温度和时间 低于引物Tm值5 ℃左右,一般在45~55℃;延伸温度和时间 72℃,1min/kb(10kb内);Tm值=4(G+C) +2(A+T);循环次数 :一般为25 ~ 30次。循环数决定PCR扩增的产量。模板初始浓度低,可增加循环数以便达到有效的 扩增量。但循环数并不是可以无限增加的。一般循环数为30个左右,循环数超过30个以后,DNA聚合酶活性逐渐达到饱和,产物的量不再随循环数的增加而增加,出现了所谓的“平台期”。聚合酶链反应可以选择这些突变来理解蛋白质是如何完成其功能的,并改变或改善蛋白质功能。

聚合酶链反应:多重连接依赖探针扩增(MLPA):允许用单个引物对扩增多个靶标,从而避免多重PCR的分辨率限制。多重聚合酶链反应:由单个PCR混合物中的多个引物组组成,以产生对不同DNA序列特异的不同大小的扩增子。通过同时靶向多个基因,可以从单次测试中获得额外的信息,否则将需要几次试剂和更多时间来执行。每个引物组的退火温度必须优化,以在单个反应中正确工作,并符合扩增子尺寸。也就是说,当通过凝胶电泳可视化时,它们的碱基对长度应该足够不同以形成不同的条带。热启动聚合酶链式反应:一种在PCR的初始建立阶段减少非特异性扩增的技术。上海分子生物学RT-PCR检测技术服务
流聚合酶链反应将溶液置于热梯度下,而不是反复加热和冷却聚合酶链反应混合物。苏州特殊样本荧光PCR
聚合酶链式反应:1976年,中国科学家,发现了稳定的Taq DNA聚合酶,为PCR技术发展也做出了基础性贡献。PCR是利用DNA在体外摄氏95°高温时变性会变成单链,低温(经常是60°C左右)时引物与单链按碱基互补配对的原则结合,标本核酸模板在提取过程中,由于吸样污染导致标本间污染;有些微生物标本尤其是病毒可随气溶胶或形成气溶胶而扩散再调温度至DNA聚合酶很适反应温度(72°C左右),DNA聚合酶沿着磷酸到五碳糖(5'-3')的方向合成互补链。基于聚合酶制造的PCR仪实际就是一个温控设备,能在变性温度,复性温度,延伸温度之间很好地进行控制。苏州特殊样本荧光PCR
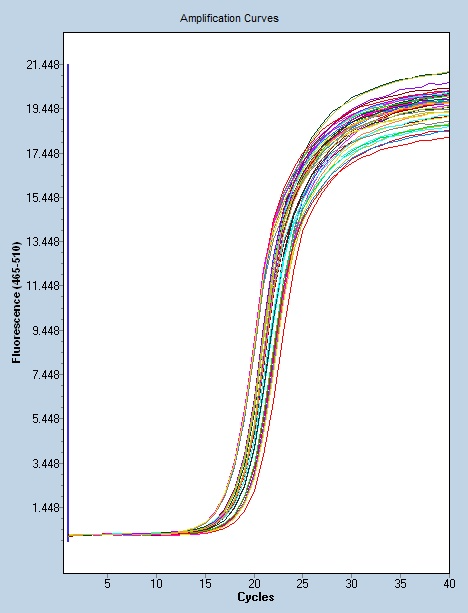
Real-time PCR从用途上分可以分为定性分析和定量分析:定量分析可以分为定量和相对定量两种。定量指的是我们想知道某个基因在初始样品中具体的拷贝数或浓度是多少?定量实验必须使用已知拷贝数的标准品,必须做标准曲线。而相对定量是指我们想知道某一个基因在不同样品中表达量的差异,其目的是测定目的基因在两个或多个样本中的含量的相对比例,而不需要知道它们在每个样本中的拷贝数。举例来说,如研究项目中包括使用高盐胁迫处理的样本和未高盐胁迫处理的样本,记为已处理样本和未处理样本,通常可以将未处理样本指定为基准,规定其目的基因浓度为100%,用已处理样本的定量结果除以未处理样本的定量结果,就可以计算每个已处...
- 厦门血液定量PCR技术服务 2024-12-25
- 宁波微量数字PCR原理及步骤 2024-12-25
- 广州组织荧光PCR供应商 2023-08-12
- 常州分子生物学定量PCR应用 2023-08-12
- 上海组织PCR检测技术方案 2023-08-11
- 珠海细胞荧光PCR原理 2023-08-11
- 武汉特殊样本荧光定量PCR原理及步骤 2023-08-10
- 南京特殊样本Real-time PCR供应商 2023-08-10
- 深圳组织荧光PCR服务 2023-08-10
- 南京细胞荧光定量PCR方案 2023-08-09
- 武汉实时Real-time PCR应用 2023-08-08
- 苏州特殊样本定量PCR哪家好 2023-08-07
- 苏州骨头数字PCR原理 2023-08-07
- 广州骨头荧光PCR服务 2023-08-07
- 连云港分子生物学定量PCR技术服务 2023-08-06
- 南通微量荧光定量PCR 2023-08-06


- 南京高表达线性PEI转染试剂注意事项 05-04
- 苏州细胞线性PEI转染试剂原理 05-04
- 深圳40000Da线性PEI转染试剂作用 05-04
- 宁波无菌线性PEI转染试剂现货 05-04
- 杭州高纯度线性PEI转染试剂服务商 05-04
- 徐州COS-7线性PEI转染试剂 05-04
- 无锡HEK-293线性PEI转染试剂厂家 05-04
- 苏州动物细胞线性PEI转染试剂价格 05-04
- 杭州高效线性PEI转染试剂使用步骤 05-04
- 深圳低毒性线性PEI转染试剂优势 05-04