随着技术的进步,病理切片染色也不断更新。近年来出现的 **多重免疫荧光(mIF)** 和 **多重免疫组化(mIHC)** 技术,使得在同一张切片上检测多个蛋白成为可能。这些方法结合数字病理和图像分析软件,可以对肿瘤免疫微环境进行***解析。此外,**空间转录组学** 和 **成像质谱** 技术的引入,使得病理切片不仅能显示组织形态,还能提供分子层面的空间信息。这些新方法正在推动病理学从传统形态学向多组学整合的方向发展。专业病理染色切片检测拍照平台。染色切片可以帮助识别病原体。普鲁士蓝染色 外包
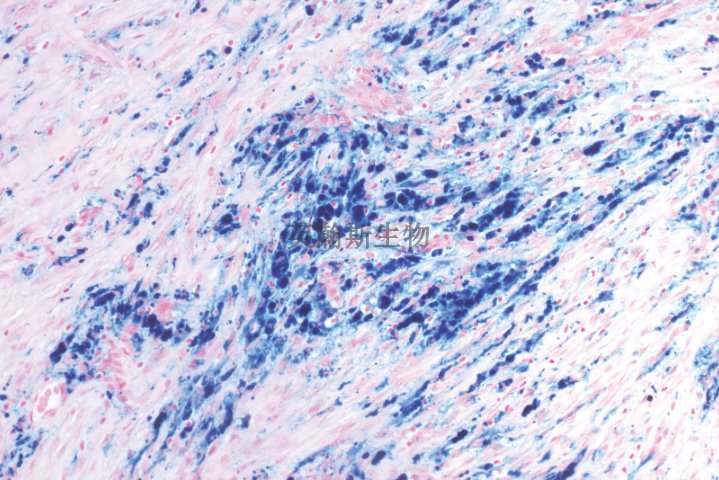
当H&E染色提示组织间质发生改变,例如怀疑存在纤维化、淀粉样变或特定细胞外基质成分沉积时,特殊染色技术便成为深化诊断的关键工具。例如,Masson三色染色通过使用不同颜色的酸性染料,能够将胶原纤维染成鲜艳的蓝色或绿色,而细胞质、肌肉纤维和角蛋白等染成红色,实现对纤维组织的精细定量和定位。这在评估肝硬化、肾小球硬化、心肌纤维化等慢性疾病的严重程度时,提供了至关重要的客观依据。另一种重要的特殊染色是刚果红(Congo Red)染色,**于检测淀粉样物质在组织中的沉积。在偏振光显微镜下,染上刚果红的淀粉样蛋白会呈现出特征性的苹果绿双折光现象,这是诊断系统性淀粉样变性的确凿证据。特殊染色是对H&E染色信息的补充和深化,它使得病理医生能够超越单纯的形态观察,直接识别和确认特定的化学成分或病理产物,从而在病因和病理生理学层面锁定疾病的本质。普鲁士蓝染色 外包染色切片可以揭示组织的微观结构和病理变化。
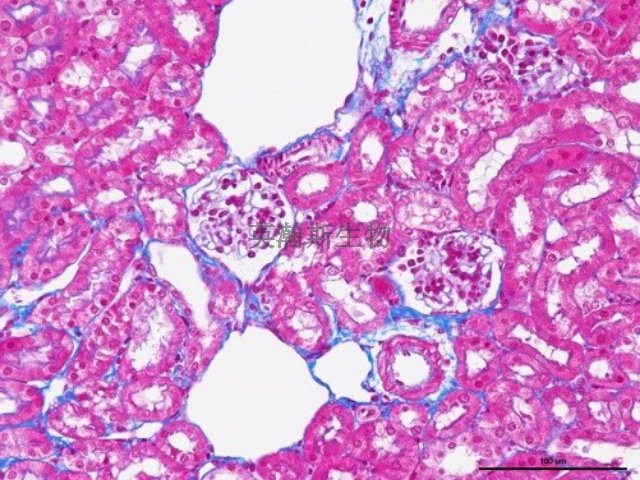
病理染色结果的可靠性直接关系到患者的生命健康,因此,染色过程的标准化和质量控制至关重要。这涉及从组织取材、固定、脱水、包埋、切片到**终染色的每一个环节。不规范的组织固定(如固定时间不足或过度)会导致细胞结构模糊或染色效果不佳;切片的厚度不均会影响染料的穿透性和结合效率;而染料的质量和配制浓度必须严格控制,定期更换,以保证染色的稳定性和可重复性。高质量的病理染色要求实验室建立严格的质量管理体系,包括定期的设备校准、试剂的批次检验,以及对染色切片的内部和外部质量评估。特别是对于IHC染色,需要设置适当的阳性和阴性对照,以验证抗体的特异性和染色系统的有效性。只有在严格的质量控制下,病理染色才能提供准确、可靠的诊断信息,确保病理报告的**性和临床指导价值。
在病理切片染色实验中,常见的问题包括 **背景染色过深**、**目标信号过弱**、**染色不均匀** 或 **组织结构脱落**。造成这些问题的原因可能是切片厚度不一致、固定不足或过度、抗体特异性不强、洗涤不彻底等。解决办法包括优化切片厚度和固定时间,选用高质量的抗体,合理设置封闭条件,以及加强洗涤步骤。此外,对于免疫染色,还需注意抗原修复条件的选择,如柠檬酸缓冲液热修复或胰蛋白酶消化,不同抗体的比较好修复方式差异很大,需要实验优化。病理学家通过染色切片分析组织变化。

病理切片染色实验的可靠性依赖于严格的质量控制。研究人员应当设置阳性对照和阴性对照,以验证染色的特异性和可靠性。阳性对照是已知表达目标抗原的组织,阴性对照则是省略一抗或使用同型对照抗体的切片。此外,重复性检测和标准化操作也十分关键。尤其在临床病理中,染色结果直接影响诊断,因此必须有统一的操作规范和评价标准。例如,IHC 中的 HER2 染色评分就是基于统一标准进行的,以保证结果的可比性和临床应用价值。专业病理切片染色拍照平台。染色切片在教学中用于展示组织学特征。普鲁士蓝染色 外包
苏丹黑B染色用于检测脂质和胆固醇。普鲁士蓝染色 外包
病理切片染色的效果在很大程度上依赖于前期的制备过程。通常包括组织取材、固定、脱水、包埋、切片和脱蜡等步骤。组织固定最常见的是 4% 多聚甲醛或 10% 中性甲醛溶液,能够保持组织结构稳定,防止自溶。石蜡包埋后使用切片机将组织切至 3–5 μm 厚度,再铺展于载玻片上。正式染色前,还需要进行脱蜡和水化,以去除石蜡并恢复组织的亲水性,为后续染色做好准备。如果这些步骤不规范,往往会导致染色不均匀或背景过重,从而影响观察结果。普鲁士蓝染色 外包