- 品牌
- 司鼎;OriCell
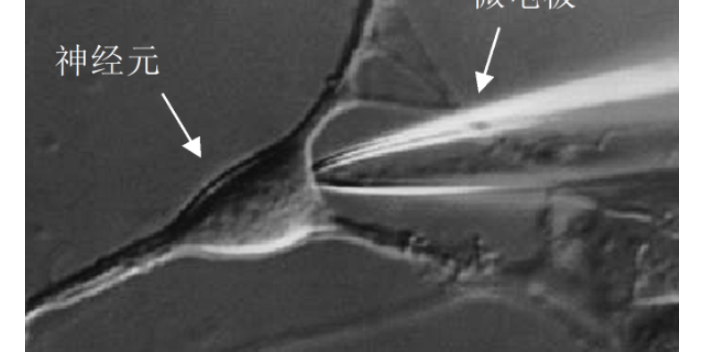
神经元膜片钳技术针对神经细胞的电活动进行测量,能够捕捉神经元膜电位和离子通道电流的微小变化。这项技术通过微电极与神经元膜形成稳定的连接,精确记录神经元的电生理信号,进而揭示神经信号传递和调控的细节。神经元作为神经系统的基本功能单位,其电活动的研究对于理解脑功能和神经疾病机制具有重要意义。膜片钳技术提供了直接观察神经元离子通道行为的方法,使研究者能够分析神经元在不同条件下的反应模式和电流特性。该技术在神经科学领域被应用于研究神经元兴奋性、突触传递以及神经网络的电生理基础,推动了对神经系统复杂功能的理解。神经元膜片钳技术的精细检测能力使其成为神经科学研究不可或缺的工具,促进了对神经细胞功能和疾病状态的深入剖析。这项技术为揭示神经系统电生理特征提供了强有力的支持,助力科学界不断推进神经科学的前沿探索。细胞功能研究,可塑性研究膜片钳技术能分析细胞特性变化规律。金华药理学脑片膜片钳技术
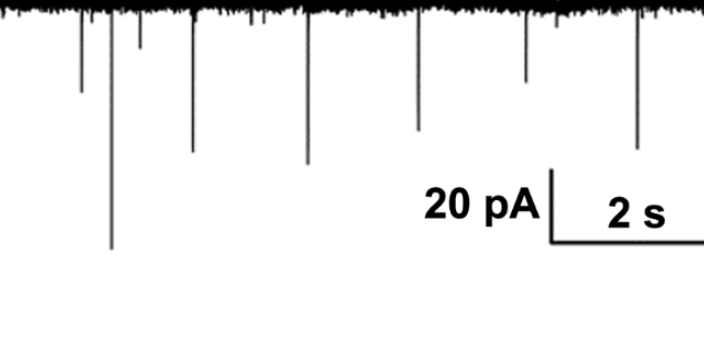
单细胞膜片钳技术是一种能够在单个细胞水平上精确测量离子通道电流的实验方法,这使得研究人员能够深入了解细胞膜上离子通道的功能特性及其调节机制。该技术通过微电极与细胞膜形成高阻抗密封,记录细胞内外电信号的变化,揭示了细胞电活动的动态过程。单细胞膜片钳技术的优势在于其能够捕捉单个细胞的电生理特征,避免了群体细胞信号的混杂,从而为揭示离子通道的多样性和异质性提供了可能。这种技术在神经科学领域尤为重要,因为神经元的功能依赖于离子通道的精细调控,单细胞膜片钳能够帮助解析神经元的信号传导机制和突触活动。此外,单细胞膜片钳技术还被应用于药物筛选过程中,通过测量药物对特定离子通道的影响,帮助确定药物的作用机制及其潜在的疗愈价值。该技术的应用不仅限于神经元,也适用于心肌细胞、内分泌细胞等多种细胞类型,促进了多领域基础研究的发展。金华药理学脑片膜片钳技术科研机构找合作,膜片钳技术服务商上海司鼎生物,提供专业支持。
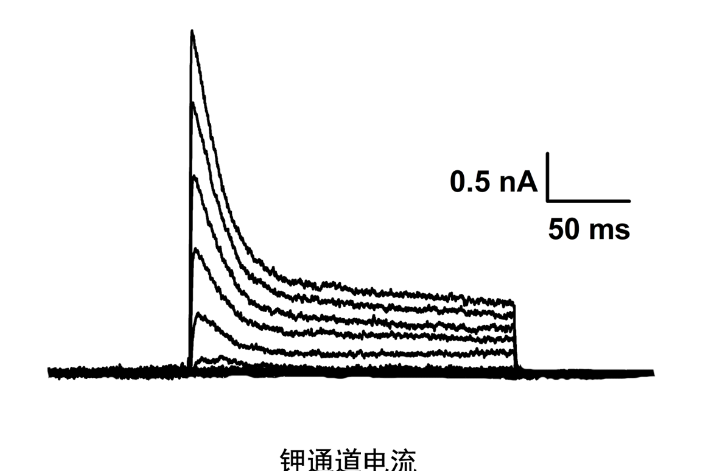
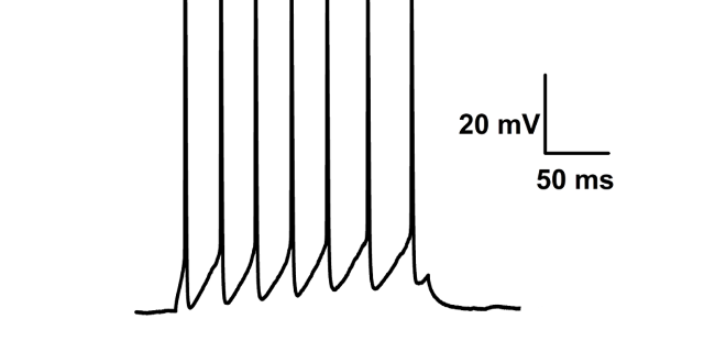
一种提高膜片钳实验效率的方法与流程:膜片钳技术是一种记录通过离子通道的离子电流来反映细胞膜上离子通道分子活动的技术。是用来研究单个离体的活细胞、组织切片或细胞膜片离子流的电生理实验技术。这项技术在可兴奋细胞如神经元、心肌细胞、肌纤维和胰腺细胞的研究中起至关重要的作用,也可用于研究特殊制备的巨型球状体中的细菌离子通道。传统膜片钳技术对实验人员的技术要求非常高,一般地,实验人员需要经过严格的长期的训练,才能准确且快速的操作。
膜片钳技术被称为研究离子通道的“金标准”。是研究离子通道的较重要的技术。目前膜片钳技术已从常规膜片钳技术(Conventionalpatchclamptechnique)发展到全自动膜片钳技术(Automatedpatchclamptechnique)。传统膜片钳技术每次只能记录一个细胞(或一对细胞),对实验人员来说是一项耗时耗力的工作,它不适合在药物开发初期和中期进行大量化合物的筛选,也不适合需要记录大量细胞的基础实验研究。全自动膜片钳技术的出现在很大程度上解决了这些问题,它不只通量高,一次能记录几个甚至几十个细胞,而且从找细胞、形成封接、破膜等整个实验操作实现了自动化,免除了这些操作的复杂与困难。这两个优点使得膜片钳技术的工作效率很大程度提高了!签于全自动膜片钳技术的这些优点,目前已经普遍的用于药物筛选。高效实验需求,高通量膜片钳技术能批量处理样本,适配大规模研究。
膜片钳技术是通过微玻管电极(膜片电极或膜片吸管)接触细胞膜,用千兆欧姆以上的阻抗使之封接,在电学上分隔和电极尖开口处相接的细胞膜的小区域(膜片)以及其周围,在此基础上固定点位,对这膜片上的离子通道的离子电流(pA级)进行监测记录的方法。测量回路的中心部分是使用场效应管运算放大器构成的I-V转换器。当场效应管运算放大器的正负输入端子是等电位,向正输入端子施加指令电位时,因为短路负端子以及膜片都可等电位地达到钳制的作用,字膜片微电极与默片之间形成10GΩ以上封接时,其间达到Z小的分流电流。借助生物学脑定位膜片钳技术,研究者能锁定特定区域细胞活动。金华药理学脑片膜片钳技术
自动化设备选品,自动化膜片钳技术推荐上海司鼎生物,效率高。金华药理学脑片膜片钳技术
膜片钳的应用:与药物作用有关的心肌离子通道:心肌细胞通过各种离子通道对膜电位和动作电位稳态的维持而保持正常的功能。国外学者在人类心肌细胞离子通道特性的研究中取得了许多进展,使得心肌药理学实验由动物细胞模型向人心肌细胞成为可能。对离子通道生理与病理情况下作用机制的研究:通过对各种生理或病理情况下细胞膜某种离子通道特性的研究,了解该离子的生理意义及其在疾病过程中的作用机制。如对钙离子在脑缺血神经细胞损害中作用机制的研究表明,缺血性脑损害过程中,Ca2+介导现象起非常重要的作用,缺血缺氧使Ca2+通道开放,过多的Ca2+进入细胞内就出现Ca2+超载,导致神经元及细胞膜损害,膜转运功能障碍,严重的可使神经元坏死。金华药理学脑片膜片钳技术
膜片钳实验中电极制备之分两次拉制,首先次拉长7~10mm,直径小于200μm,在此基础上进行第二次拉制,较终使尖锐端的直径为1~2μm,两步拉制的目的主要是使电极前端的锥度变大,狭窄部长度缩短,因此可降低电极的串联电阻,也可减少全细胞记录时的电极液透析时间。由于膜片微电极较忌沾染灰尘和脏物,更忌触碰尖锐端附近部位,所以一般要求在使用前制作。抛光:将电极固定于显微镜工作台上,在镜下将尖锐端靠近加热丝,当通电加热时,可见电极尖锐端微微回缩,此时电极变得光滑,且尖锐端的杂质烧去,得到较干净的表面。从而有利于和细胞膜紧密封接,并在封接后更易保持稳定。单细胞分析常结合膜片钳技术获取个体电信号,让研究者更...
- 南通医学脑定位膜片钳网站 2026-03-20
- 芜湖药理学实用膜片钳哪家好 2026-03-19
- 温州医学膜片钳 2026-03-19
- 南京医学膜片钳实验设计公司 2026-03-18
- 福州药理学脑定位膜片钳方案 2026-03-17
- 黄山神经生物学脑定位膜片钳应用 2026-03-16
- 苏州全自动膜片钳全细胞记录技术 2026-03-16
- 合肥细胞生物学膜片钳成像原理 2026-03-14
- 东莞细胞生物学实用膜片钳服务 2026-03-14
- 莆田细胞生物学实用膜片钳 2026-03-13
- 湖州神经生物学脑定位膜片钳技术 2026-03-07
- 东莞药理学膜片钳实验设计公司 2026-03-07
- 宁波细胞生物学实用膜片钳原理 2026-03-06
- 无锡神经生物学电生理膜片钳原理及步骤 2026-03-05
- 连云港药理学膜片钳方案 2026-03-05
- 厦门药理学脑片膜片钳哪家好 2026-03-04


- 福州药理学脑定位膜片钳方案 03-17
- 黄山神经生物学脑定位膜片钳应用 03-16
- 苏州全自动膜片钳全细胞记录技术 03-16
- 合肥细胞生物学膜片钳成像原理 03-14
- 东莞细胞生物学实用膜片钳服务 03-14
- 莆田细胞生物学实用膜片钳 03-13
- 莆田全自动膜片钳成像原理 03-13
- 无锡神经生物学离子通道方案 03-12
- 药理学实用膜片钳哪家好 03-11
- 嘉兴药理学膜片钳电生理技术方案 03-10