阿尔茨海默病实验动物模型。目前常用研究AD的实验动物有非人灵长类动物与啮齿类动物,在选择时遵循“减少、替代、优化”的3R原则。非人灵长类动物与人类的脑部解剖结构、神经病变特点以及生物行为模式相似,尤其是恒河猴,在其脑中观察到含有Aβ沉积的老年斑和神经原纤维缠结现象,无论是自发还是诱发模型,都能够较好的复制AD相关的病理及生理特征,但是昂贵的费用与稀少的资源限制了非人灵长类动物的大量应用。啮齿类动物虽然在病变模拟方面不如非人灵长类全方面的,但是具有价格低廉、资源范围很广的、生存率高等特点,与人类的脑部解剖结构与生理特征也较为相近,更适于诱导模型的大量制备,成为AD应用更范围很广的的动物模型。许多AD小鼠模型的背景品系是C57BL/6J小鼠,然而这种品系的小鼠似乎对类似AD的神经病理学具有特别的抵抗力。实验动物模型价格多少?新疆推荐实验动物模型外包
阿尔茨海默病的实验动物模型之化学损伤动物模型。主要是以向模型鼠脑部、皮下或腹腔注射特定物质来建立模型,如通过立体定位仪、微透析等方法向实验动物脑内海马、基底核、侧脑室等不同部位注入Aβ片段,鹅蒿蕈氨酸(IBO)、STZ等物质。或通过皮下或腹腔注射D-半乳糖、三氯化铝、冈田酸(OKA)和东莨菪碱(SCOP)等致损物质。Aβ诱导模型,Aβ诱导模型是通过在海马CA1区或者侧脑室多次注射Aβ片段诱发Aβ沉积、形成SP为主要病理特点的AD动物模型。Aβ诱导的AD动物模型脑内Aβ沉积明显、Aβ斑块周围星形胶质细胞增生,行为呆滞,易卧,学习记忆能力衰退,出现认知功能障碍、体能衰减明显等AD病理表现。Aβ诱导动物模型,影响因素单一,模型形成时间长,造模过程中,有对脑组织造成穿透性损伤的不确定性,另外,由于注射部位过于集中,使Aβ沉积部位与AD患者Aβ在脑内多区域分布有所不同。甘肃制作实验动物模型制作方法英瀚斯生物,承接小鼠实验动物模型。
双转基因实验动物模型。利用基因打靶技术培育出的APP/PS-1双转基因鼠,在3月龄时出现学习记忆障碍、Aβ增多和形成SP,6月龄时即可出现严重的学习记忆力衰退、认知功能障碍,神经元变性和突触丢失等多种AD病理特性。对AD 病理特征Aβ和SP方面的研究主要采用APP/PS-1双转基因鼠。但其外源性基因表达不够稳定性、动物价格高。
APP/PS1/Tau 三转因模型。APP/PS1/Tau 三转基因小鼠模型是由APPSwe、PS1、TauP301L基因系突变建立的,首先在皮质区和出现Aβ异常沉积、SP 和NFTs 形成,随后海马区也逐渐出现 Aβ沉积、SP和NFTs,以及突触丢失、神经元变性AD临床病理表现。APP/PS1/Tau三转基因小鼠模型是目前与AD 病理特征接近的转基因动物模型,但其外源性基因表达稳定性较差、造模较困难且造价高。
诱导性实验动物模型诱导性实验动物模型是通过药物、手术、环境因素或病原体等外界刺激,使实验动物在短时间内表现出类似人类疾病的特征。例如,使用四氧嘧啶或链脲佐菌素(STZ)破坏胰岛β细胞,可以诱导糖尿病模型;通过高脂饲料喂养动物,可以构建高脂血症或非酒精性脂肪肝模型。此外,脑缺血再灌注模型通常采用大脑中动脉栓塞(MCAO)的方法来模拟脑卒中。相比自发性模型,诱导性模型具有更好的可控性和可重复性,能够在较短时间内形成稳定的病理状态。然而,这类模型可能不能完全再现疾病的所有特征,因此需要结合其他研究方法进行验证。实验动物模型构建服务就找英瀚斯。
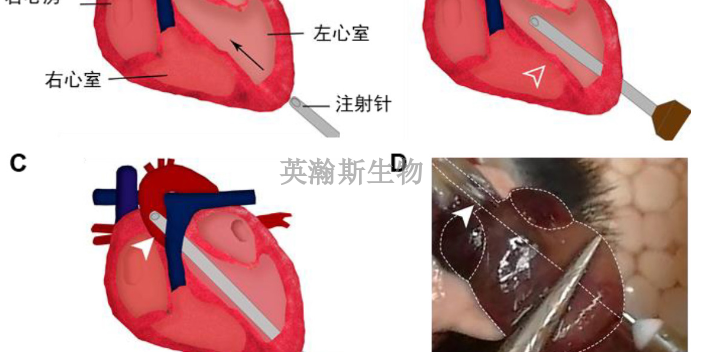
实验动物模型是指以实验动物为载体,模拟医学、生命科学、食品安全和军shi医学等科学研究,以及生物医药和健康产品研发中应用的与人类疾病、功能紊乱发生机制和临床表现高度相似的生物样本。实验动物模型是我国科学研究、生物医药和健康产品研发中不可替代的核xin生物资源,在提高我国自主创新能力、发展医药卫生健康产业等方面具有重要的现实意义和广阔的市场前景。南京英瀚斯生物科技有限公司的团队实体组建于2013年,是专注于医学科研外包服务的国家高新技术企业。实验动物模型基因敲除、表性分析。安徽好的实验动物模型外包
英瀚斯生物,真实做实验动物模型,可实地参观考察。新疆推荐实验动物模型外包
转基因实验动物模型
转基因实验动物模型是利用基因工程技术,使特定基因在动物体内过表达或抑制表达,以研究基因功能及其与疾病的关系。这类模型***用于**、神经退行性疾病和代谢疾病的研究。例如,APP/PS1双转基因小鼠是一种经典的阿尔茨海默病模型,表现出β-淀粉样蛋白沉积和认知功能障碍。转基因小鼠在特定基因的调控下,可以精细模拟疾病的分子机制,为靶向***提供了可靠的研究基础。然而,转基因动物的构建通常耗时长、成本高,且可能存在非预期的基因表达变化,影响实验结果的稳定性。 新疆推荐实验动物模型外包