有研究发现,杆状病毒表达载体体系BEV生产的rAAV发生了与293生产体系不同的衣壳蛋白翻译后修饰(post-translationalmodifications,PTMs)。这一差异是否会影响载体趋向性和转导效率还需要进一步验证。除此之外,杆状病毒多重infection会导致载体蛋白VP1、VP2和VP3比例不一致。尽管如此,BEV/Sf9系统仍然是一种颇有吸引力的大规模临床级载体生产策略。随着以后对基因药物需求的增加,AAV载体的需求量也会与日俱增,而BEV系统能够降低AAV的成本,未来还是很有发展潜力的。SAN HQ高盐核酸酶具有热不稳定的特性,在还原剂存在条件下,50℃、30min孵育即可失活;四川体外诊断高盐核酸酶70921-150

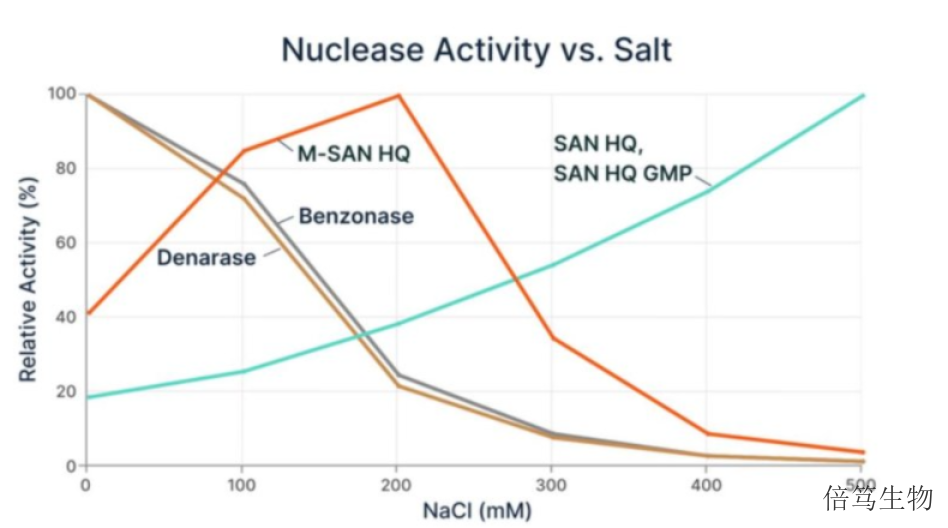
已有文献表明,高盐浓度能够破坏染色质结构,让核小体解聚。在能耐受高盐条件的病毒载体(如AdV/AAV等)生产中,高盐浓度使宿主细胞DNA(HCD)解聚,让核酸片段暴露,提高了核酸片段的可及性。而ArcticZymes的SAN HQ高盐核酸酶能够在高盐条件下更好发挥酶切活性,作为高盐条件下去除HCD的更好选择。SAN HQ高盐核酸酶的出现,让一些通过常规方法很难解决的工艺问题得到高效解决,不仅提高了生产效率,降低了药物生产成本,更拓宽了生物工艺生产的边界。四川体外诊断高盐核酸酶70921-150衢州高盐核酸酶服务哪家好呢,欢迎咨询上海倍笃生物 。
近年来,AAV在cancer疾病的医治中显示出巨大的价值。AAV作为基因药物的载体已在肺、肝、眼、脑、肌肉等多个临床试验(超过100次)中得到应用,并在盲症和血友病方面取得了巨大成功。2012年,AAV1载体编码的脂蛋白脂肪酶成为欧盟批准的shou个用于医治脂蛋白脂肪酶缺乏症的基因产物(Glybera)。5年后,另一种AAV介导的基因药物(Luxturna)随后获准在美国上市。基于AAV9的基因疗(Zolgensma)也被用于医治脊髓性肌肉萎缩。腺病毒在基础和实验研究有这么强的生命力原因在于:宿主范围广,对人致病率低;腺病毒粒子相对稳定,病毒基因重排频率低;安全性高,不整合到染色体中,无插入致病基因,不干扰其他宿主基因。
ArcticZymes Technologies于2017年推出了SAN HQ高盐核酸酶及其对应的SAN HQ ELISA kit。该试剂盒原理是采用双抗夹心法定量检测各种生物制品的中间品、半成品和成品中SAN HQ高盐核酸酶的残留含量,特异性的anti-SAN作为捕获抗体偶联在96-well plate,生物素Biotin标记anti-SAN作为检测抗体,链霉亲和素-HRP偶联物起到信号放大作用,TMB是终反应底物。该试剂盒特异识别SAN HQ高盐核酸酶,对其它核酸酶没有特异性结合。它的定量范围是0.4-25.6ng/ml,检测精确度高RSD<=15%,2-8℃条件下保存12个月。SAN HQ高盐核酸酶能够使载体表面的DNA去除更彻底,得到的AAV病毒颗粒更稳定。
残留的宿主DNA是生产中产生的杂质,其存在潜在的致瘤性、传染性和免疫原性等风险。相关研究表明,基因的大小普遍在200bp以上,因此大于200bp有可能会有一定的致病性,而且残留DNA片段越大,生物制品的风险等级越高。因此,各国监管机构对其提出了严格要求。美国食品药品监督管理局(FDA)在《关于人类基因zhiliao新产品生产指导文件》中明确指出HCD的片段要小于200bp。2022年5月,国家药品监督管理局药品评审中心(CDE)发布的《体内基因药物产品药学研究与评价技术指导原则(试行)》中也明确指出需对DNA残留量和残留片段大小进行控制,建议尽量将DNA残留片段的大小控制在200bp以下。常州高盐核酸酶价格哪家好呢,欢迎咨询上海倍笃生物 。浙江基因药物生产用高盐核酸酶70921
SAN HQ高盐核酸酶促进残留DNA的消化,有助于符合FDA要求。四川体外诊断高盐核酸酶70921-150
监管部门对HCD的残留量有明确的规定。美国FDA发布的指导原则中指出生物制品HCD残余限度为 100pg/剂,对于大剂量生物制品如单克隆抗体,根据其残留DNA来源及给药途径,残留量可放宽至 10ng/剂。细胞基因药物终产品的DNA残留有两种来源,分别是宿主细胞DNA(HCD)和转染用的质粒。质粒和HCD的存在形式不同,去除效率也差别很大。其中,质粒是裸露的DNA双链,带强负电荷,通过色谱纯化主要是离子交换能够很高效去除;HCD则是以核小体紧密折叠形成的染色质形式存在,几乎不以裸DNA形式存在,所以很难去除。四川体外诊断高盐核酸酶70921-150
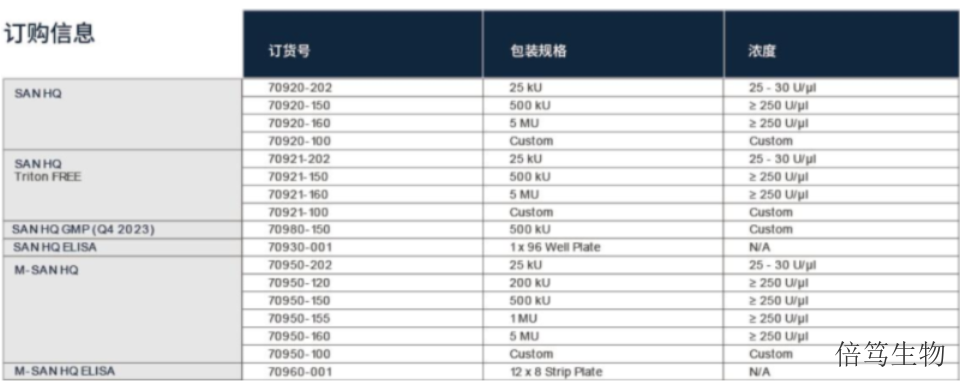
市售的SAN HQ高盐核酸酶有三个规格,分别是25kU、500kU及5MU,分别满足研发初期及大规模...
【详情】氯化铯(CsCl)/碘克沙醇密度梯度离心大概是经典的AAV纯化技术了。这种技术适用于所有血清型且分辨...
【详情】基因药物是指将外源基因引入靶细胞,纠正或补偿基因缺陷或异常引起的疾病的。这种策略对许多疾病的康复有很...
【详情】宿主细胞DNA残留的担忧是基于致ai风险理论,特别是生产细胞系所包含的致ai序列,比如较常见腺病毒基...
【详情】由于Triton X-100的降解产物对环境影响很大,自2023年12月22日起,欧盟将禁止使用Tr...
【详情】氯化铯(CsCl)/碘克沙醇密度梯度离心大概是经典的AAV纯化技术了。这种技术适用于所有血清型且分辨...
【详情】ArcticZymes厂家对盐活性核酸酶系列产品(Salt Active Nucleases,SAN...
【详情】ArcticZymes Technologies致力于提供高质量产品,具有良好的批间一致性、稳定可靠...
【详情】SANHQ(生物工艺级)是用Pichiapastoris表达的重组非特异性内切核酸酶,广泛应用于生产...
【详情】离子交换层析 (IEC) 是一种简单、通用且经济高效的技术,已成为许多载体纯化的关键步骤。IEC分为...
【详情】残留的宿主DNA是生产中产生的杂质,其存在潜在的致瘤性、传染性和免疫原性等风险。相关研究表明,基因的...
【详情】SANHQ(生物工艺级)是用Pichiapastoris表达的重组非特异性内切核酸酶,广泛应用于生产...
【详情】